
近来众多研究表明肠道菌群失调可以通过肠-脑轴影响阿尔茨海默病(AD)进程,其过程涉及宿主免疫、神经、代谢调节。而微生物可受到多种因素影响,如饮食等环境因素、宿主遗传变异等遗传因素。现有研究支持宿主遗传变异不仅可以直接作用于宿主表型,也可通过调控肠道菌群,进而影响AD进程。因此,解析AD复杂发病机制需要同时考虑遗传因素和肠道菌群的影响。
本团队总共收集了252例中国人的粪便样本和血液样本作为发现队列,分别进行宏基因组、全基因组测序,其涵盖了AD发展的5个阶段。首先,利用LDA主题模型,将发现队列的肠道微生物组成由15个肠道社团特征表征。其中,Topic_8菌群社团丰度与AD病程进展一致的连续下降趋势,并在两个独立验证队列(自产中国人重复队列+一个公共日本队列)复现,说明其关联模式的鲁棒性。进一步探索菌群社团(Topic_8)的物种组成,厌氧链球菌(54%)作为主导菌,因此我们将该社团命名为富集厌氧链球菌“社团”,简写为ES-Ana。
接着,通过整合人体宿主基因型数据,对ES-Ana丰度进行GWAS分析,我们发现了41个与肠道ES-Ana丰度相关的独立宿主遗传变异。我们计算个体的AD多基因风险评分,分数越高表示患AD的风险越大,发现AD的多基因风险评分与肠道ES-Ana丰度、认知得分显著负相关。因此,我们强调肠道ES-Ana丰度与AD病程进展具有显著遗传关联,对AD有保护作用。
我们将41个关联SNP基于位置进行基因注释,共鉴定了174个ES-Ana相关基因,含与AD相关的基因。这些基因显著富集在AD相关的生物功能和疾病表型上,说明其与AD的潜在关联。进一步描绘相关基因在不同细胞类型中差异表达,我们发现相关基因多在AD病人胶质细胞中显著低表达,其中AD差异表达基因(如APOE,TENM2 )与脑内脂质代谢、神经发育等密切相关。
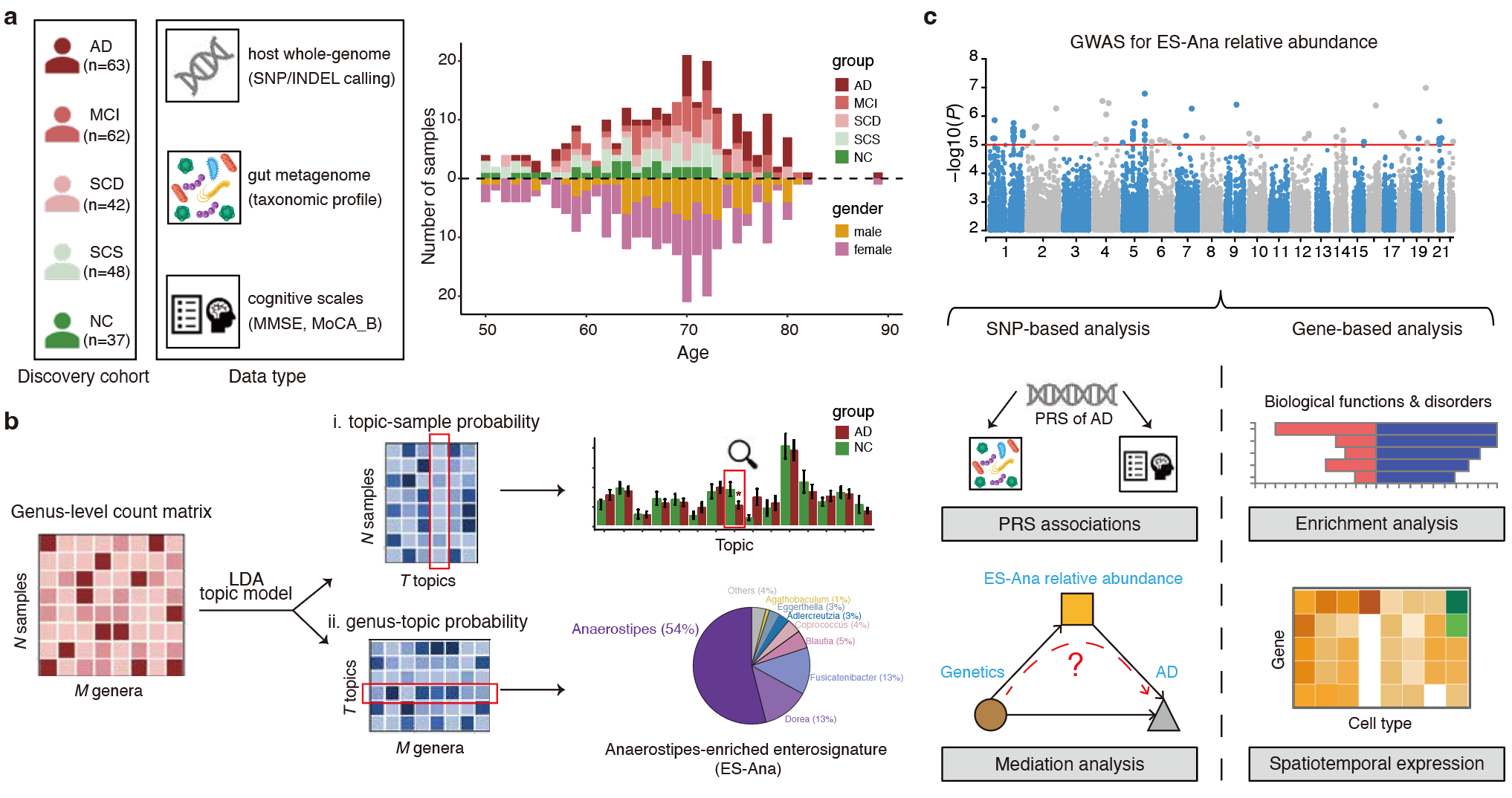
图:实验设计
总之, 我们的研究揭示了AD中肠道微生物群变化的复杂遗传效应,并为肠-脑轴在AD中的作用提供了新的证据。
这一项成果以《Impacts of host genetics on gut microbiome composition in Alzheimer’s disease》为题,已于2026年3月5日发表在Microbiome期刊。复旦大学博士生刘金鑫为本文第一作者,复旦大学赵兴明教授、杨禹丞副研究员为本论文共同通讯。该论文受到国家重点研发计划、国家自然科学基金委、上海市科技委员会等经费资助。
原文链接:https://link.springer.com/article/10.1186/s40168-026-02342-8