
2025年11月28日,复旦大学生物医学工程与技术创新学院赵兴明教授、类脑智能科学与技术研究院陈靖祺副研究员团队在Science Bulletin发表题为“Characterizing schizophrenia-relevant structural variants and tandem repeats through long-read sequencing”的论文。
结构变异(structural variants, SVs)是指影响碱基数超过50bp的遗传变异,被认为是人类基因组多样性以及多种疾病风险的重要遗传基础。近年来,大量研究表明,罕见结构变异——包括拷贝数变异和串联重复扩增——在精神分裂症的遗传风险和神经生物学机制中发挥重要作用。然而,传统的二代测序技术由于读长较短,难以准确检测大型或位于重复区域的结构变异,从而限制了我们对精神分裂症遗传风险的系统性认识。
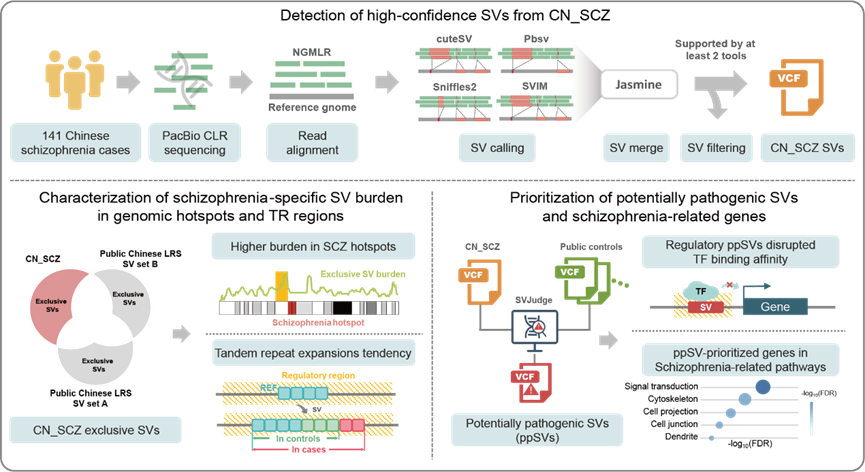
图:实验设计
基于所述背景,研究团队开展了基于三代长读长测序(long-read sequencing, LRS)的精神分裂症结构变异研究。该研究共纳入141名中国精神分裂症患者,开发了跨队列筛选与功能优先级排序的综合分析框架,通过整合公共对照数据,对疾病队列特异出现和潜在致病的结构变异进行了系统分析。
研究发现,中国精神分裂症队列特异出现的结构变异在与精神分裂症相关的热点区域负担显著提高。例如,在广泛被报道与精神分裂症和神经发育障碍相关的16p12.1区域内,观察到了超预期的疾病队列特异性结构变异的富集。除此之外,这些特异性的结构变异还反映了位于编码区域和调控区域的串联重复扩增倾向,而这类复杂区域往往难以通过二代测序进行精确映射。利用团队自主开发的结构变异致病性评估工具SVJudge,共鉴定出358个潜在致病的结构变异(potentially pathogenic SVs, ppSVs),其中许多与基因组调控元件和重复区域重叠。功能分析表明,197个ppSVs影响了转录因子结合活性,扰动了在脑组织及神经元相关细胞中活跃的调控关系,并影响多种已知的精神分裂症风险基因及其治疗药物靶点。例如,在与神经发育相关的基因CBL和RAC1启动子区域发现了潜在致病性插入,这些变异增强了对应区域的转录因子结合强度,并影响多种已知精神分裂症药物的靶点。最终,基于ppSVs共鉴定了82个候选风险基因,包括59个已知的精神分裂症相关基因和23个新发现的基因,这些基因在神经发育和突触功能通路中显著富集。这些发现有助于理解结构变异在精神分裂症风险中的作用机制,并提供了潜在的干预靶标。
总体而言,本研究提供了首个针对中国精神分裂症群体的长读长测序资源,系统解析了该疾病中结构变异的遗传特征,拓展了对精神分裂症遗传风险因素的认识,并展示了长读长测序在揭示复杂疾病难解遗传机制上的广阔应用前景。
复旦大学赵兴明教授和陈靖祺副研究员为共同通讯作者,博士研究生安政宇为该论文的第一作者。该工作得到了国家重点研发计划(2023YFF1204800,2020YFA0712403)、国家自然科学基金委员会(T2225015,62433008,32200537)、上海市科学技术委员会项目(23JS1410100,24JS2810100)、上海市教育委员会项目(24KXZNA11)、海南省重点科技项目(ZDYF2024SHFZ058)以及广州国家实验室专项项目(GZNL2024A01003)的资助。