
随着全球老龄化进程加速,阿尔茨海默病(AD)带来的医疗保健负担越来越沉重。AD是最常见的神经退行性疾病,具有长达十年的临床前病理期。新证据表明,肠道菌群可以通过“微生物群-肠-脑轴”影响神经炎症、β-淀粉样蛋白沉淀和tau蛋白磷酸化等临床前病理过程,有望为AD的早期无创诊断提供新途径。然而, AD进展中肠道菌群的变化尚未得到很好的表征,其作为诊断标志物的能力有待进一步评估。
近日,复旦大学类脑智能科学与技术研究院赵兴明教授团队联合多家单位,基于张江国际脑库(ZIB)神经退行性疾病队列, 通过多阶段、大规模肠道菌群研究,揭示了AD进展中广泛的肠道菌群变化,并验证了其作为无创诊断标志物的能力。相关成果以《Metagenomic analysis characterizes stage-specific gut microbiota in Alzheimer's disease》为题,于2025年3月31日发表在Nature旗下精神病学领域高水平期刊Molecular Psychiatry。
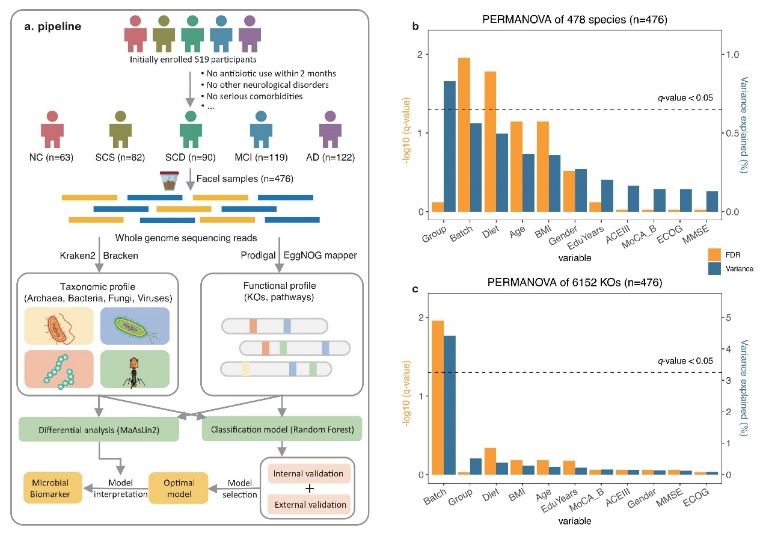
研究团队对476名中国受试者进行深度粪便宏基因组测序,构建了迄今为止最大的AD多阶段肠道菌群数据集。研究团队首先揭示了AD进展过程中广泛的肠道菌群失调,发现部分差异丰度菌与神经炎症、神经递质失调等AD病理事件密切相关。研究团队进一步发现基于微生物基因家族的分类模型表现出强大的诊断能力,证明了肠道菌群作为AD无创诊断标志物的可行性。研究团队还通过粪便微生物群移植,证明肠道菌群能够影响AD中认知功能衰退的进展,提示粪菌移植或将成为延缓疾病进展的有效策略。
复旦大学类脑智能科学与技术研究院博士生贾龙豪、复旦大学生命科学学院博士生柯溢泽为本文共同第一作者。复旦大学类脑智能科学与技术研究院赵兴明教授,复旦大学中山医院丁晶教授,复旦大学生命科学学院吴浩教授以及上海大学生命科学学院王娇副教授为本文通讯作者。该论文受到国家重点研发计划、国家自然科学基金委、上海市科技委员会、上海市科技重大专项、临港实验室等经费资助。